Doelen¶
In hoofdstukken 5 en 6 van het boek wordt er verder ingegaan op de reversibiliteit van processen. De klassieke mechanica eist alleen behoud van energie en impuls, maar er is geen richtingsvoorkeur in processen. Dat is in strijd met je dagelijkse ervaring: van een video-opname kun je vrijwel altijd zeggen of deze vooruit of achteruit wordt gespeeld.
Deze richtingsvoorkeur wordt het best gemodelleerd door de entropie. Dit is een kwantitatieve grootheid die vaak een beetje mysterieus wordt gevonden. In dit werkblad zullen we kijken of we wat meer over deze entropie te weten kunnen komen.
In dit werkblad komen de volgende onderdelen langs:
We herhalen de belangrijke stukken code met gekozen constanten en het gedrag van deeltjes.
We introduceren een nieuwe klasse voor het beheersvolume die de reeds ontwikkelde functies bevat.
We controleren of deze code gelijkwaardige resultaten geeft als de code in voorgaande werkbladen.
We bekijken een ingewikkelder modelsysteem van gekoppelde zuigers en kijken hier naar verschillende processen.
We nemen een reversibele en een niet-reversibele route en kijken naar het verschil in entropie.
Laden van eerdere code¶
Net als bij de eerdere simulaties, gaan we uit van dezelfde set van constanten.
import numpy as np
import matplotlib.pyplot as plt
from matplotlib.animation import FuncAnimation
FAST_MODE = True # Zet op False voor de volledige (langzamere) simulatie
FAST_MAX_STEPS = 6000 # cap voor lange loops (snelle modus)
# ----------------------------
# Constanten (gekozen zodat T ≈ 300 K en diameter ≈ 0.1 nm)
# ----------------------------
k_B = 1.38e-23 # J/K
MASS = 4.65e-26 # kg (orde van grootte luchtmolecuul)
T0 = 300 # K
BOX_SIZE_0 = 20e-9 # m (hoogte en lengte startvolume)
N = 30 if FAST_MODE else 40
RADIUS = 0.05e-9 # m (diameter 0.1 nm)
# kies V_0 zodat de kinetische energie overeenkomt met T0 (2D: <E_kin> = k_B T)
V_0 = np.sqrt(2 * k_B * T0 / MASS)
# tijdstap
DT = 1.0e-13 # s
# startsnelheid van zuiger (negatief betekent beide zuigers naar binnen)
V_PISTON_0 = (-0.08 if FAST_MODE else -0.02) * V_0
# reproduceerbaarheid
np.random.seed(0)En maken we daarnaast ook gebruik van een klasse die het gedrag van deeltjes omschrijft:
class ParticleClass:
def __init__(self, m, v, r, R):
""" maakt een deeltje (constructor) """
self.m = m
self.v = np.array(v, dtype=float)
self.r = np.array(r, dtype=float)
self.R = R
def update_position(self):
""" verandert positie voor één tijdstap """
self.r += self.v * DT
@property
def momentum(self):
return self.m * self.v
@property
def kin_energy(self):
return 1/2 * self.m * np.dot(self.v, self.v)
def collide_detection(p1: ParticleClass, p2: ParticleClass) -> bool:
""" Geeft TRUE als de deeltjes overlappen """
dx = p1.r[0] - p2.r[0]
dy = p1.r[1] - p2.r[1]
rr = p1.R + p2.R
return dx**2+dy**2 < rr**2
def particle_collision(p1: ParticleClass, p2: ParticleClass):
""" past snelheden aan uitgaande van overlap """
m1, m2 = p1.m, p2.m
delta_r = p1.r - p2.r
delta_v = p1.v - p2.v
dot_product = np.dot(delta_r, delta_v)
# Als deeltjes van elkaar weg bewegen dan geen botsing
if dot_product >= 0: # '='-teken voorkomt ook problemen als delta_r == \vec{0}
return
distance_squared = np.dot(delta_r, delta_r)
# Botsing oplossen volgens elastische botsing in 2D
p1.v -= 2 * m2 / (m1 + m2) * dot_product / distance_squared * delta_r
p2.v += 2 * m1 / (m1 + m2) * dot_product / distance_squared * delta_rHet beheersvolume¶
In het boek wordt er vaak gesproken over een ‘control volume’. Dit is een reëel of denkbeeldig volume waaraan een aantal macroscopische eigenschappen worden toegekend. Het Nederlandse woord hiervoor is ‘beheersvolume’. Veel van de functies die we tot nu toe hebben ontwikkeld gaan over eigenschappen en gedrag van een dergelijk beheersvolume - deze hebben we slechts impliciet gebruikt. Om de code beter te structureren, maken we hier een klasse voor. Dit maakt het vooral makkelijk om bijvoorbeeld met twee beheersvolumes te rekenen (later in dit werkblad is dat ons doel).
Als je de code hieronder vergelijkt met die van de vorige werkbladen, zal je een aantal zaken opvallen:
Elke functie heeft een parameter
selfgekregen. Daarmee begrijpt Python dat het om een functie van de klasse gaat.De variabelen die als
globalstonden vermeld zijn nu een variabele van de klasse en hoeven dus niet meer gedeclareerd te worden in elke functie. Ze moeten in de code wel telkens worden voorafgegaan door het woordself, om dit duidelijk te maken.Om de eigenschappen
heat,workenpressurealleen te laten lezen en niet te laten schrijven, maken we gebruik van een Python conventie waarbij we een ‘geheime’ variabele gebruiken die wordt voorafgegaan door een laag liggend streepje ‘_’ (Engels: underscore).
class ControlVolume:
def __init__(self, length, height, N, v_piston, set_temp):
""" maakt een beheersvolume (constructor) """
self.length = length
self.height = height
self.v_piston = v_piston
self.set_temp = set_temp
self.particles = []
self._work = 0.0
self._heat = 0.0
self._impulse_out = 0.0
self._pressure = 0.0
for _ in range(N):
vx = np.random.uniform(-V_0, V_0)
vy = np.random.choice([-1, 1]) * np.sqrt(V_0**2 - vx**2)
x = np.random.uniform(-self.length/2 + RADIUS, self.length/2 - RADIUS)
y = np.random.uniform(-self.height/2 + RADIUS, self.height/2 - RADIUS)
self.particles.append(ParticleClass(m=MASS, v=[vx, vy], r=[x, y], R=RADIUS))
def handle_collisions(self) -> None:
""" alle onderlinge botsingen afhandelen voor deeltjes in lijst """
num_particles = len(self.particles)
for i in range(num_particles):
for j in range(i+1, num_particles):
if collide_detection(self.particles[i], self.particles[j]):
particle_collision(self.particles[i], self.particles[j])
def piston_collision(self, particle: ParticleClass) -> None:
""" verzorgen van botsingen met wand links en rechts, die als zuiger kunnen bewegen """
if abs(particle.r[0]) + particle.R > self.length / 2:
particle.r[0] = np.sign(particle.r[0]) * (self.length/2 - particle.R)
piston_velocity = np.sign(particle.r[0]) * self.v_piston
relative_velocity = particle.v[0] - piston_velocity # stelsel zuiger
particle.v[0] = -relative_velocity + piston_velocity # stelsel waarnemer
self._impulse_out += 2 * particle.m * abs(relative_velocity)
self._work += 2 * particle.m * relative_velocity * piston_velocity
def thermostat_collision(self, particle: ParticleClass) -> None:
""" verzorgen van botsingen met wand boven en onder, die als thermostaat kunnen werken """
if abs(particle.r[1]) + particle.R > self.height / 2:
temp_factor = (self.set_temp/self.temperature) if self.set_temp > 0 else 1.0
particle.r[1] = np.sign(particle.r[1]) * (self.height/2 - particle.R)
self._impulse_out += abs(particle.momentum[1]) * (1 + temp_factor**0.5)
self._heat += particle.kin_energy * (temp_factor - 1)
particle.v *= temp_factor**0.5
particle.v[1] *= -1
def handle_walls(self) -> None:
""" verzorgen van alle botsingen met wanden en aanpassen waarde voor druk """
self._impulse_out = 0.0
for p in self.particles:
self.piston_collision(p)
self.thermostat_collision(p)
self._pressure = 0.95 * self._pressure + 0.05 * self._impulse_out / (self.circumference * DT)
def take_time_step(self) -> None:
self.length += 2 * self.v_piston * DT # zowel links als rechts zuiger
for p in self.particles:
p.update_position()
self.handle_collisions()
self.handle_walls()
@property
def temperature(self) -> float:
# In 2D geldt per deeltje: <E_kin> = k_B T
if len(self.particles) == 0:
return 0.0
total_ke = 0.0
for p in self.particles:
total_ke += p.kin_energy
temp = total_ke / (len(self.particles) * k_B)
return temp
@property
def area(self) -> float:
return self.length * self.height
@property
def circumference(self) -> float:
return 2 * (self.length + self.height)
@property
def heat(self) -> float:
return self._heat
@property
def work(self) -> float:
return self._work
@property
def pressure(self) -> float:
return self._pressure
Herhaling oude test¶
Om zeker te zijn dat de code functioneert herhalen we eerst een berekening, waarvan we het antwoord al kennen. Dit is de simulatie van de druk en de temperatuur als functie van het volume voor een isotherm proces (waarbij de temperatuur dus constant wordt gehouden met behulp van een thermostaat).
num_steps = round(2/3 * BOX_SIZE_0 / (2 * -V_PISTON_0 * DT))
volumes = np.zeros(num_steps, dtype=float)
pressures = np.zeros(num_steps, dtype=float)
temperatures = np.zeros(num_steps, dtype=float)
cv = ControlVolume(BOX_SIZE_0, BOX_SIZE_0, 40, V_PISTON_0, 300)
for i in range(num_steps):
cv.take_time_step()
volumes[i] = cv.area
pressures[i] = cv.pressure
temperatures[i] = cv.temperature
fig, (ax1, ax2) = plt.subplots(1, 2, figsize=(9, 3))
ax1.set_xlabel('Volume')
ax1.set_ylabel('Pressure')
ax2.set_xlabel('Volume')
ax2.set_ylabel('Temperature')
fig.tight_layout
ax1.plot(volumes, pressures, '-r')
ax2.plot(volumes, temperatures, '-b')
plt.show()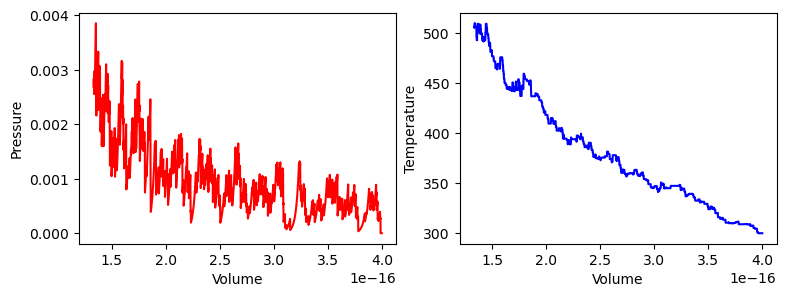
Systeem van twee gekoppelde zuigers¶
Om nu een studie te doen naar de entropie van een systeem maken we gebruik van twee gekoppelde zuigers, zie Figure 1. Dit zijn twee zuigers genummerd ‘1’ en ‘2’ die samen een constant volume hebben, maar waarbij de beweging van de zuiger(s) het ene volume verkleint en het andere volume evenveel vergroot. Dit systeem houden we voor de rest van dit weerkblad thermisch geïsoleerd ten opzichte van de omgeving, zodat we een goede boekhouding kunnen doen van de totale hoeveelheid energie.

Figure 1:De gekoppelde zuigers, waarbij het totaal volume constant is.
Isotherme verplaatsing¶
Als eerste kijken we naar het reversibele proces. We herhalen dat er geen thermisch contact is met de omgeving, maar er is wel thermisch contact tussen de twee volumes zodat ze constant dezelfde temperatuur hebben.
In de onderstaande code beginnen we met twee beheersvolumes cv1 en cv2, die aan het begin hetzelfde volume hebben.
Dan verplaatsen we de zuiger(s) met een constante snelheid naar het punt waar en (wat verwacht je, conceptueel, wat er gebeurt met de verschillende grootheden?)
Hieronder vind je het verloop van de druk en de temperatuur van beide volumes tijdens dit proces.
# runnen van de simulatie
num_data = round(abs(BOX_SIZE_0 * 0.4 / (DT * V_PISTON_0)))
if FAST_MODE:
num_data = min(num_data, FAST_MAX_STEPS)
volumes1 = np.zeros(num_data, dtype=float)
pressures1 = np.zeros(num_data, dtype=float)
temperatures1 = np.zeros(num_data, dtype=float)
volumes2 = np.zeros(num_data, dtype=float)
pressures2 = np.zeros(num_data, dtype=float)
temperatures2 = np.zeros(num_data, dtype=float)
cv1 = ControlVolume(BOX_SIZE_0, BOX_SIZE_0, (30 if FAST_MODE else 50), +V_PISTON_0, 0.5)
cv2 = ControlVolume(BOX_SIZE_0, BOX_SIZE_0, (30 if FAST_MODE else 50), -V_PISTON_0, 0.5)
for i in range(num_data):
cv1.take_time_step()
cv2.take_time_step()
average_temp = (cv1.temperature + cv2.temperature) / 2
cv1.set_temp = average_temp
cv2.set_temp = average_temp
volumes1[i] = cv1.area
pressures1[i] = cv1.pressure
temperatures1[i] = cv1.temperature
volumes2[i] = cv2.area
pressures2[i] = cv2.pressure
temperatures2[i] = cv2.temperature# plotten van de druk en temperatuur van beide volumes
fig, (ax1, ax2) = plt.subplots(1, 2, figsize=(9, 3))
ax1.set_xlabel('Volume')
ax1.set_ylabel('Pressure')
ax2.set_xlabel('Volume')
ax2.set_ylabel('Temperature')
fig.tight_layout
#druk als functie van volume
ax1.plot(volumes1, pressures1, '-r', label='cv1')
ax1.plot(volumes2, pressures2, '-m',label='cv2')
ax1.legend()
#temperatuur als functie van volume
ax2.plot(volumes1, temperatures1, '-b',label='cv1')
ax2.plot(volumes2, temperatures2, '-g',label='cv2')
ax2.legend()
plt.show()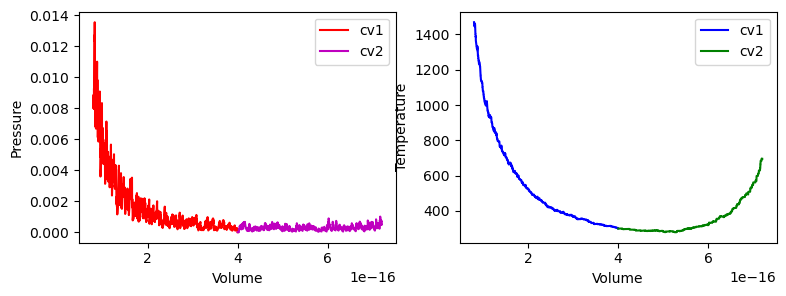
{solution} ex-entropy-04
Als de zuiger uitwijkt, wordt het ene volume kleiner en het andere groter. Omdat stijgt de druk aan de kleine kant; om de zuiger verder te verplaatsen moet er netto arbeid op het totale systeem worden verricht.
Die arbeid gaat naar de interne energie, dus stijgt en daarmee ook .
Voor grotere uitwijking wordt het volume van de kleine kant heel klein, waardoor sterk toeneemt en de benodigde arbeid per extra stap groter wordt. Dat zie je ook in de afleiding:
waarbij de factor snel groter wordt als .
Dit systeem is zo gekozen dat het mogelijk is om de temperatuur analytisch te bepalen met behulp van een wiskundige afleiding.
We gaan ervan uit dat het systeem bij de start helemaal symmetrisch is (zoals in de simulatie) en definiëren hierbij als de positie van de zuiger.
Bij staat de zuiger helemaal aan de kant van cv1, zodat en .
Bij staat de zuiger helemaal aan de andere kant, zodat en .
Dan moet dus gelden dat:
Omdat ons gas twee vrijheidsgraden heeft, wordt de interne energie van elk van de volumes () gegeven door:
Met het aantal deeltjes aan beide kanten gelijk betekent dit voor de interne energie van het totale systeem
Voor het verplaatsen van de zuiger geldt voor beide kanten:
Als we deze twee formules samennemen dan levert dit:
Vullen we de startformules voor en in, dan wordt dit:
{solution} ex-entropy-06
We kiezen als systeem het totale gekoppelde systeem (cv1 + cv2) en nemen aan dat er geen warmte-uitwisseling is met de omgeving. Dus .
Met de eerste hoofdwet volgt dan direct:
De warmte die in de code tussen cv1 en cv2 “verplaatst” wordt is intern en telt voor het totale systeem niet als warmte naar de omgeving.
# Theorie: dT/dx = x/(1-x^2) T => T(x) = T0 / sqrt(1 - x^2)
# x uit de volumes (totaal volume constant)
x = (volumes1 - volumes2) / (volumes1 + volumes2)
T_avg = 0.5 * (temperatures1 + temperatures2)
T0_sim = T_avg[0]
T_theory = T0_sim / np.sqrt(1 - x**2)
plt.figure(figsize=(7,4))
plt.plot(x, temperatures1, '.', ms=3, alpha=0.4, label='cv1 (sim)')
plt.plot(x, temperatures2, '.', ms=3, alpha=0.4, label='cv2 (sim)')
plt.plot(x, T_theory, '-', lw=2, label='theorie $T_0/\sqrt{1-x^2}$')
plt.xlabel('$x$')
plt.ylabel('$T$')
plt.legend()
plt.show()
print(f"T0 (sim) ≈ {T0_sim:.2f}")
print(f"T_theorie(x=-0.8) ≈ {T0_sim/np.sqrt(1-0.8**2):.2f}")
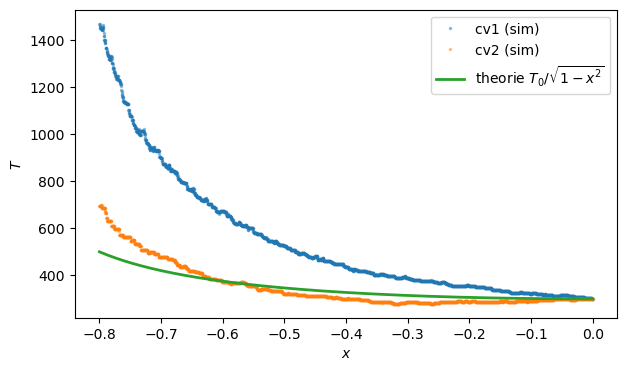
T0 (sim) ≈ 300.00
T_theorie(x=-0.8) ≈ 500.00
Om te verifiëren dat dit proces reversibel is moeten we het proces ook terug kunnen uitvoeren.
# Beweeg de zuiger terug en vergelijk heen- en terugweg
# begin vanuit de eindtoestand van de vorige simulatie (cv1 en cv2 bestaan al)
cv1.v_piston *= -1
cv2.v_piston *= -1
num_back = num_data
volumes1_back = np.zeros(num_back, dtype=float)
temperatures1_back = np.zeros(num_back, dtype=float)
volumes2_back = np.zeros(num_back, dtype=float)
temperatures2_back = np.zeros(num_back, dtype=float)
for i in range(num_back):
cv1.take_time_step()
cv2.take_time_step()
average_temp = (cv1.temperature + cv2.temperature) / 2
cv1.set_temp = average_temp
cv2.set_temp = average_temp
volumes1_back[i] = cv1.area
temperatures1_back[i] = cv1.temperature
volumes2_back[i] = cv2.area
temperatures2_back[i] = cv2.temperature
x_fwd = (volumes1 - volumes2) / (volumes1 + volumes2)
x_back = (volumes1_back - volumes2_back) / (volumes1_back + volumes2_back)
T_fwd = 0.5 * (temperatures1 + temperatures2)
T_back = 0.5 * (temperatures1_back + temperatures2_back)
plt.figure(figsize=(7,4))
plt.plot(x_fwd, T_fwd, '-', label='heenweg')
plt.plot(x_back, T_back, '--', label='terugweg')
plt.xlabel('$x$')
plt.ylabel('$T$')
plt.legend()
plt.show()
print(f"Start (heen): x≈{x_fwd[0]:.3f}, T≈{T_fwd[0]:.2f}")
print(f"Einde (terug): x≈{x_back[-1]:.3f}, T≈{T_back[-1]:.2f}")
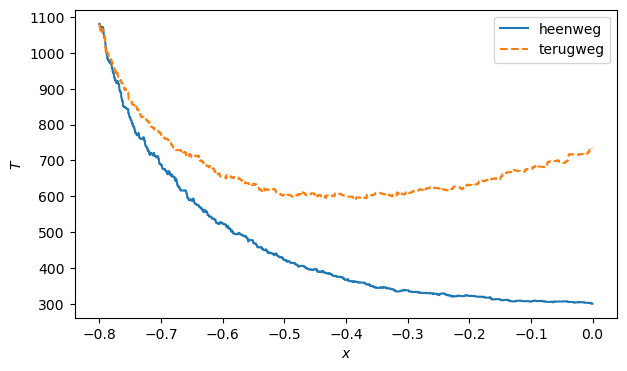
Start (heen): x≈-0.000, T≈300.00
Einde (terug): x≈0.000, T≈732.59
Adiabatische verplaatsing zuiger¶
We kunnen in een vergelijkbare eindsituatie komen door de zuiger eerst adiabatisch te verplaatsen (dat wil zeggen: zonder onderling thermisch contact tussen de volumes) en pas daarna het thermische contact toe te staan. Om dat in onze simulatie te modelleren concentreren we ons eerst op de adiabatische verplaatsing van de zuigerwand en nemen we het thermische contact nog niet mee.
ex-entropy-11
Voor een 2D ideaal (monoatomisch) gas geldt (want en per deeltje).
Bij een adiabatisch proces geldt:
We verplaatsen naar , dus
Daarmee:
```{exercise}
:label: ex-entropy-12
Maak een code voor een adiabatische verplaatsing voor de zuigerwand van de positie $x=0$ naar de positie $x=-0.8$.
Je kan hiervoor het best starten vanuit de code voor het isotherme proces en deze aanpassen.# Adiabatische verplaatsing: geen thermisch contact tijdens het bewegen
# => zet set_temp = 0 zodat de thermostaat niets doet (temp_factor = 1)
num_data = round(abs(BOX_SIZE_0 * 0.4 / (DT * V_PISTON_0)))
if FAST_MODE:
num_data = min(num_data, FAST_MAX_STEPS)
volumes1_ad = np.zeros(num_data, dtype=float)
temperatures1_ad = np.zeros(num_data, dtype=float)
volumes2_ad = np.zeros(num_data, dtype=float)
temperatures2_ad = np.zeros(num_data, dtype=float)
cv1 = ControlVolume(BOX_SIZE_0, BOX_SIZE_0, (30 if FAST_MODE else 50), +V_PISTON_0, 0.0) # cv1 wordt kleiner
cv2 = ControlVolume(BOX_SIZE_0, BOX_SIZE_0, (30 if FAST_MODE else 50), -V_PISTON_0, 0.0) # cv2 wordt groter
T0_ad = 0.5 * (cv1.temperature + cv2.temperature)
for i in range(num_data):
cv1.take_time_step()
cv2.take_time_step()
volumes1_ad[i] = cv1.area
temperatures1_ad[i] = cv1.temperature
volumes2_ad[i] = cv2.area
temperatures2_ad[i] = cv2.temperature
x_ad = (volumes1_ad - volumes2_ad) / (volumes1_ad + volumes2_ad)
plt.figure(figsize=(7,4))
plt.plot(x_ad, temperatures1_ad, '-', label='cv1 (adiabatisch)')
plt.plot(x_ad, temperatures2_ad, '-', label='cv2 (adiabatisch)')
plt.xlabel('$x$')
plt.ylabel('$T$')
plt.legend()
plt.show()
# Theoretische verwachting voor 2D ideaal gas: γ = 2 => T V^(γ-1) = T V = const
V0 = BOX_SIZE_0 * BOX_SIZE_0
T1_pred = T0_ad * (V0 / (0.2*V0))
T2_pred = T0_ad * (V0 / (1.8*V0))
print(f"T0 ≈ {T0_ad:.2f}")
print(f"Sim eind: T1≈{temperatures1_ad[-1]:.2f}, T2≈{temperatures2_ad[-1]:.2f}")
print(f"Theorie: T1≈{T1_pred:.2f} (=5 T0), T2≈{T2_pred:.2f} (=5/9 T0)")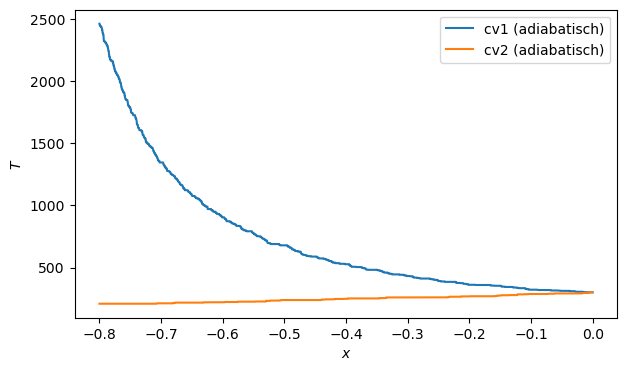
T0 ≈ 300.00
Sim eind: T1≈2465.38, T2≈208.15
Theorie: T1≈1500.00 (=5 T0), T2≈166.67 (=5/9 T0)
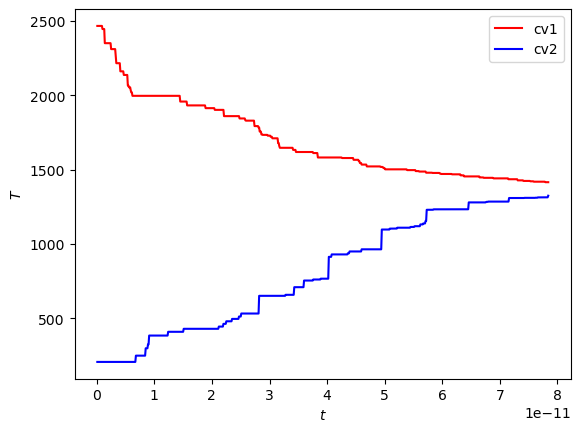
Na de adiabatische verplaatsing moeten de twee volumes alsnog in thermisch evenwicht gebracht worden. Dat doen we met de code hieronder.
times = []
temp1 = []
temp2 = []
average_temp = (cv1.temperature + cv2.temperature) / 2
cv1.set_temp = average_temp
cv2.set_temp = average_temp
cv1.v_piston = 0.0
cv2.v_piston = 0.0
time = 0.0
max_iter = 5000 if FAST_MODE else 200000
iter_count = 0
while (cv2.temperature < 0.99 * cv2.set_temp) and (iter_count < max_iter):
time += DT
iter_count += 1
cv1.take_time_step()
cv2.take_time_step()
temp1.append(cv1.temperature)
temp2.append(cv2.temperature)
times.append(time)
if iter_count >= max_iter:
print('Let op: maximaal aantal stappen bereikt; evenwicht mogelijk nog niet volledig (FAST_MODE).')
plt.figure()
plt.xlabel('$t$')
plt.ylabel('$T$')
plt.plot(times, temp1, '-r', label='cv1')
plt.plot(times, temp2, 'b-', label='cv2')
plt.legend()
plt.show()
Vergelijk van de twee experimenten¶
We hebben de zuiger in twee experimenten verschoven:
We begonnen in toestand 0, waarbij de zuiger in het midden stond en naar toestand 1 bewoog, met thermisch contact tussen de twee volumes.
We begonnen in toestand 0 en verplaatsten de zuiger zonder thermisch contact (adiabatisch) naar toestand 2. Daarna brachten we de twee volumes in thermisch contact en zonder volumeverandering naar evenwicht kwamen in toestand 3.
Deze processen zijn schematisch weergegeven in Figure 2.

Figure 2:Schematische weergave van de twee processen in een -diagram met de verschillende toestanden genummerd weergegeven.
Uit de thermodynamische formules en uit de simulatie kun je concluderen dat de eindtemperatuur na deze twee experimenten verschillend is. Omdat we het systeem nooit in thermisch contact met de omgeving hebben gebracht, moet de energie hiervoor uit de arbeid komen die de zuigerwand heeft verricht. Dit laat zien dat de arbeid die nodig is van de ene in de andere toestand te komen, afhankelijk is van het gekozen proces.
ex-entropy-16 We kiezen als systeem steeds het totale systeem (cv1 + cv2), zonder warmte-uitwisseling met de omgeving. Dan geldt:
Proces 0 → 1 (met thermisch contact tijdens bewegen)
De theorie geeft bij :
Totale interne energie: (met het aantal deeltjes per volume).
Dus:
Proces 0 → 2 → 3 (adiabatisch bewegen, daarna alleen warmte-uitwisseling bij stilstaande zuiger)
Na de adiabatische stap:
en dus
Start: .
Dus:
De stap 2→3 heeft geen arbeid (zuiger staat stil), dus .
Verschil in verrichte arbeid
Met in de simulatie per volume en :
Een reversibele route is dan het 'goedkoopste' proces om in een toestand te komen. Voor het experiment zou het perfect uitgevoerde isotherme proces reversibel zijn en daarom de laagste temperatuur opleveren bij $x=-0.8$.
```{exercise} entropy production
:label: ex-entropy-17
Bereken uit de theoretische, thermodynamische formules hoeveel entropie er vrijkomt bij het tweede proces. ex-entropy-17
De entropieproductie is gelijk aan de totale entropieverandering van het geïsoleerde systeem (er is geen warmte-uitwisseling met de omgeving).
Voor een 2D ideaal gas geldt per volume:
Voor toestand 0: , .
Voor toestand 3: , , .
Sommeer voor beide volumes:
Omdat , valt dit mooi samen:
Dus de geproduceerde entropie is:
Willen we maximale arbeid halen in de stap van toestand 2 naar toestand 3, dan kunnen we dat doen met twee reversibele warmtepompen die de twee beheersvolumes koppelen aan een denkbeeldig bad. Entropie is een toestandsgrootheid, zodat de entropieproductie in dit proces net zo groot moet zijn als in onze zuiger van daarnet. Voor een reversibel proces zoals we met deze warmtepompen uitvoeren is er geen entropieproductie. Dan moet er dus gelden dat:
Als we de omgevingstemperatuur op een waarde stellen van dan moet er dus gelden:
Dit betekent dat het systeem tijdens dit reversibele proces deze hoeveelheid moet accepteren van de omgeving om de eindtoestand te bereiken.
Omdat we daarnaast van de eerste hoofdwet weten dat:
en er moet gelden dat de interne energie van het systeem niet verandert tijdens dit temperatuurverloop kunnen we concluderen dat:
In het proces dat bij onze simulatie heeft plaatsgevonden is er geen enkele arbeid door het systeem uitgevoerd. We zien dus dat de entropie die we in dit geval hebben berekend een maat is voor de arbeid die we hadden kunnen winnen door op dezelfde eindtoestand te komen via een reversibel proces.
We kunnen dit ook andersom zeggen: de hoeveelheid entropie die tijdens het proces gecreëerd wordt is een maat voor de hoeveelheid beschikbare arbeid die we tijdens het proces hebben verloren door het niet perfect reversibel uit te voeren.